Articles
- Page Path
- HOME > J Korean Acad Nurs > Volume 56(1); 2026 > Article
-
Research Paper
성인 중환자실 환자의 중증도 보정지수에 따른 사망 예측 도구 유용성과 사망 영향요인: 후향적 의무기록 조사연구 -
이재정
 , 김동연
, 김동연 , 이민지
, 이민지 , 김지영
, 김지영
- Usefulness of Charlson comorbidity index-adjusted mortality prediction tools and factors influencing mortality in intensive care unit patients: a retrospective medical record review–based study
-
Jai Jung Lee
 , Dong Yeon Kim
, Dong Yeon Kim , Min Ji Lee
, Min Ji Lee , Ji Young Kim
, Ji Young Kim
-
Journal of Korean Academy of Nursing 2026;56(1):27-38.
DOI: https://doi.org/10.4040/jkan.25094
Published online: February 11, 2026
가톨릭대학교 서울성모병원 간호부
Nursing Department, Seoul St. Mary’s Hospital, The Catholic University of Korea, Seoul, South Korea
- Corresponding author: Dong Yeon Kim Nursing Innovation Unit, The Catholic University of Korea, Seoul St. Mary’s Hospital, 222 Banpo-daero, Seocho-gu, Seoul 06591, South Korea E-mail: vonma98@naver.com
© 2026 Korean Society of Nursing Science
This is an Open Access article distributed under the terms of the Creative Commons Attribution NoDerivs License (http://creativecommons.org/licenses/by-nd/4.0) If the original work is properly cited and retained without any modification or reproduction, it can be used and re-distributed in any format and medium.
- 2,158 Views
- 222 Download
Abstract
-
Purpose
- This study aimed to estimate the mortality rate in adult intensive care units (ICUs) using the Charlson comorbidity index (CCI)-adjusted Acute Physiology and Chronic Health Evaluation (APACHE) II and Simplified Acute Physiology Score (SAPS) III models, and to identify factors influencing mortality.
-
Methods
- This retrospective cohort study included adult patients admitted to the ICU at a tertiary hospital between June 1 and August 31, 2022. Among the 1,098 screened patients, those younger than 18 years, those discharged within 48 hours, and those with missing medical records were excluded. In total, 482 patients were analyzed using the chi-square test, independent t-test, and multivariate logistic regression. Model performance was evaluated using the c-statistic and the Hosmer-Lemeshow goodness-of-fit test.
-
Results
- The predictive accuracy of the mortality models was shown by concordance statistic (C-statistic) values of .817 for APACHE II, .857 for SAPS III, .697 for CCI, and .834 for CCI-adjusted APACHE II. Mechanical ventilation, cardiopulmonary cerebral resuscitation, continuous renal replacement therapy, and the presence of leukemia or lymphoma were significant predictors of mortality in adult ICU patients. Among the evaluated models, SAPS III and CCI-adjusted APACHE II demonstrated the highest predictive power.
-
Conclusion
- The findings indicate that incorporating comorbidity indices such as the CCI with acute physiological parameters improves the accuracy of mortality prediction in ICU patients. Understanding mortality prediction models is essential for nurses to provide individualized, evidence-based, and high-quality care in adult ICUs.
서론
방법
1) 환자의 일반적인 특성
2) Acute Physiology and Chronic Health Evaluation II
3) Simplified Acute Physiology Score III
4) 중증도 보정지수(Charlson comorbidity index)
결과
고찰
결론
-
Conflicts of Interest
No potential conflict of interest relevant to this article was reported.
-
Acknowledgements
This study is reported according to the Strengthening the Reporting of Observational Studies in Epidemiology (STROBE) statement.
-
Funding
This study was supported by the research fund of Seoul St. Mary’s Hospital, The Catholic University of Korea.
-
Data Sharing Statement
Please contact the corresponding author for data availability.
-
Author Contributions
Conceptualization or/and Methodology: JL, DYK, MJL, JYK. Data curation or/and Analysis: JL, DYK, MJL, JYK. Funding acquisition: JL, DYK. Investigation: JL, DYK, MJL, JYK. Project administration or/and Supervision: JL, DYK. Resources or/and Software: JL, DYK. Validation: JL, DYK, MJL, JYK. Visualization: JL, DYK, MJL, JYK. Writing: original draft or/and Review & Editing: JL, DYK. Final approval of the manuscript: all authors.
Article Information
Values are presented as number (%) or mean±standard deviation.
BMI, body mass index; COVID-19, coronavirus disease 2019; CPCR, cardiopulmonary cerebral resuscitation; CRRT, continuous renal replacement therapy; DNR, do not resuscitate; ECMO, extracorporeal membrane oxygenation; ER, emergency room; ICU, intensive care unit; LST, life-sustaining treatment.
| Mortality prediction models | C-statistics | pa) |
|---|---|---|
| SAPS III | .857 | .576 |
| APACHE II | .817 | .729 |
| CCI | .692 | .118 |
| SAPS III+CCI | .857 | .543 |
| APACHE II+CCI | .834 | .128 |
Nagelkerke R2=0.57, χ2=208.08, p<.001, hit ratio=82.0%; Hosmer-Lemeshow Goodness of fit χ2=3.64, p=.888.
APACHE, Acute Physiology and Chronic Health Evaluation; CCI, Charlson Comorbidity Index; CI, confidence interval; CPCR, cardiopulmonary cerebral resuscitation; CRRT, continuous renal replacement therapy; ECMO, extracorporeal membrane oxygenation; OR, odds ratio; SAPS, Simplified Acute Physiology Score; SE, standard error; VIF, variance inflation factor.
- 1. Jeong AI, Shin S, Hong E. Factors related to workload of intensive care unit nurses: systematic review and meta-analysis. J Korean Clin Nurs Res. 2023;29(3):296-311. https://doi.org/10.22650/JKCNR.2023.29.3.296Article
- 2. Go UR, Cho SH. Relationship between patient classification system and APACHE II scores, and mortality prediction in a surgical intensive care unit. J Korean Acad Nurs Adm. 2024;30(1):67-78. https://doi.org/10.11111/jkana.2024.30.1.67Article
- 3. Chung J, Ahn J, Ryu JA. Beyond SOFA and APACHE II, novel risk stratification models using readily available biomarkers in critical care. Diagnostics (Basel). 2025;15(9):1122. https://doi.org/10.3390/diagnostics15091122ArticlePubMedPMC
- 4. Ghazaly HF, Aly AA, Sayed MH, Hassan MM. APACHE IV, SAPS III, and SOFA scores for outcome prediction in a surgical/trauma critical care unit: an analytical cross-sectional study. Ain-Shams J Anesthesiol. 2023;15:101. https://doi.org/10.1186/s42077-023-00383-xArticle
- 5. Le Gall JR, Lemeshow S, Saulnier F. A new Simplified Acute Physiology Score (SAPS II) based on a European/North American multicenter study. JAMA. 1993;270(24):2957-2963. https://doi.org/10.1001/jama.270.24.2957ArticlePubMed
- 6. Hong CS, Jang DH. Validation ratings for the length of the ROC curve. Korean Data Inf Sci Soc. 2020;31(5):851-863. https://doi.org/10.7465/jkdi.2020.31.5.851Article
- 7. Moreno RP, Metnitz PG, Almeida E, Jordan B, Bauer P, Campos RA, et al. SAPS 3: from evaluation of the patient to evaluation of the intensive care unit: Part 2: development of a prognostic model for hospital mortality at ICU admission. Intensive Care Med. 2005;31(10):1345-1355. https://doi.org/10.1007/s00134-005-2763-5ArticlePubMedPMC
- 8. Moreno R, Vincent JL, Matos R, Mendonça A, Cantraine F, Thijs L, et al. The use of maximum SOFA score to quantify organ dysfunction/failure in intensive care: results of a prospective, multicentre study. Working Group on Sepsis related Problems of the ESICM. Intensive Care Med. 1999;25(7):686-696. https://doi.org/10.1007/s001340050931ArticlePubMed
- 9. Lemeshow S, Teres D, Avrunin JS, Gage RW. Refining intensive care unit outcome prediction by using changing probabilities of mortality. Crit Care Med. 1988;16(5):470-477. https://doi.org/10.1097/00003246-198805000-00002ArticlePubMed
- 10. Lemeshow S, Teres D, Klar J, Avrunin JS, Gehlbach SH, Rapoport J. Mortality Probability Models (MPM II) based on an international cohort of intensive care unit patients. JAMA. 1993;270(20):2478-2486. https://doi.org/10.1001/jama.1993.03510200084037ArticlePubMed
- 11. Higgins TL, Teres D, Copes WS, Nathanson BH, Stark M, Kramer AA. Assessing contemporary intensive care unit outcome: an updated Mortality Probability Admission Model (MPM0-III). Crit Care Med. 2007;35(3):827-835. https://doi.org/10.1097/01.CCM.0000257337.63529.9FArticlePubMed
- 12. Knaus WA, Zimmerman JE, Wagner DP, Draper EA, Lawrence DE. APACHE-acute physiology and chronic health evaluation: a physiologically based classification system. Crit Care Med. 1981;9(8):591-597. https://doi.org/10.1097/00003246-198108000-00008ArticlePubMed
- 13. Knaus WA, Draper EA, Wagner DP, Zimmerman JE. APACHE II: a severity of disease classification system. Crit Care Med. 1985;13(10):818-829. https://doi.org/10.1097/00003246-198510000-00009ArticlePubMed
- 14. The APACHE III prognostic system. Risk prediction of hospital mortality for critically ill hospitalized adults. Chest. 1991;100(6):1619-1636. https://doi.org/10.1378/chest.100.6.1619ArticlePubMed
- 15. Zimmerman JE, Kramer AA, McNair DS, Malila FM. Acute Physiology and Chronic Health Evaluation (APACHE) IV: hospital mortality assessment for today’s critically ill patients. Crit Care Med. 2006;34(5):1297-1310. https://doi.org/10.1097/01.CCM.0000215112.84523.F0ArticlePubMed
- 16. Lee H, Choi EY, Kim YH. Validation of APACHE II score and comparison of the performance of APACHE II and adjusted APACHE II models in a surgical intensive care unit. Korean J Crit Care Med. 2011;26(4):232-237. https://doi.org/10.4266/kjccm.2011.26.4.232Article
- 17. Kang CH, Kim YI, Lee EJ, Park K, Lee JS, Kim Y. The variation in risk adjusted mortality of intensive care units. Korean J Anesthesiol. 2009;57(6):698-703. https://doi.org/10.4097/kjae.2009.57.6.698ArticlePubMed
- 18. Charlson ME, Pompei P, Ales KL, MacKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chronic Dis. 1987;40(5):373-383. https://doi.org/10.1016/0021-9681(87)90171-8ArticlePubMed
- 19. de Haan E, van Oosten B, van Rijckevorsel VA, Kuijper TM, de Jong L, Roukema GR. Validation of the Charlson comorbidity index for the prediction of 30-day and 1-year mortality among patients who underwent hip fracture surgery. Perioper Med (Lond). 2024;13(1):67. https://doi.org/10.1186/s13741-024-00417-4ArticlePubMedPMC
- 20. Shin DW, Han K. The use of Charlson comorbidity index for observational studies using administrative data in Korea. Precis Future Med. 2025;9(1):2-14. https://doi.org/10.23838/pfm.2024.00191Article
- 21. Stavem K, Hoel H, Skjaker SA, Haagensen R. Charlson comorbidity index derived from chart review or administrative data: agreement and prediction of mortality in intensive care patients. Clin Epidemiol. 2017;9:311-320. https://doi.org/10.2147/CLEP.S133624ArticlePubMedPMC
- 22. Yoo CS, Sim MY, Choi EH. Development of Korean patient classification system for critical care nurses. J Korean Clin Nurs Res. 2015;21(3):401-411. https://doi.org/10.22650/JKCNR.2015.21.3.401Article
- 23. Kim H, Kim K. Verification of validity of MPM II for neurological patients in intensive care units. J Korean Acad Nurs. 2011;41(1):92-100. https://doi.org/10.4040/jkan.2011.41.1.92ArticlePubMed
- 24. Yu X, Ouyang L, Li J, Peng Y, Zhong D, Yang H, et al. Knowledge, attitude, practice, needs, and implementation status of intensive care unit staff toward continuous renal replacement therapy: a survey of 66 hospitals in central and South China. BMC Nurs. 2024;23(1):281. https://doi.org/10.1186/s12912-024-01953-6ArticlePubMedPMC
- 25. Moridani MK, Setarehdan SK, Nasrabadi AM, Hajinasrollah E. A predictive model of death from cerebrovascular diseases in intensive care units. Intell Med. 2023;3(4):267-279. https://doi.org/10.1016/j.imed.2023.01.005Article
- 26. Kim S, No MJ, Moon KE, Cho HJ, Park Y, Lee NJ, et al. Intensive care unit nurses’ death perception, end of life stress and end of life nursing attitudes. J Korean Clin Nurs Res. 2018;24(2):255-262. https://doi.org/10.22650/JKCNR.2018.24.2.255Article
- 27. Kim KH. Comorbidity adjustment in health insurance claim database. Health Policy Manag. 2016;26(1):71-78. https://doi.org/10.4332/kjhpa.2016.26.1.71Article
- 28. Oh TK, Song IA. Trained intensivist coverage and survival outcomes in critically ill patients: a nationwide cohort study in South Korea. Ann Intensive Care. 2023;13(1):4. https://doi.org/10.1186/s13613-023-01100-5ArticlePubMedPMC
- 29. Karagiannis P, Klingler F, Arelin V, Alsdorf W, König C, Roedl K, et al. Outcome of critically ill patients receiving systemic chemotherapy on the intensive care unit. Front Oncol. 2024;14:1508112. https://doi.org/10.3389/fonc.2024.1508112ArticlePubMedPMC
- 30. Otten M, van Kempen BJ, van der Woude B, Dam TA, Gigengack RK, Müller MC, et al. Long-term mortality in ICU patients with hematological malignancies: Impact of organ support duration and ICU length of stay. J Crit Care. 2025;89:155122. https://doi.org/10.1016/j.jcrc.2025.155122ArticlePubMed
- 31. Tsang M, LeBlanc TW. Palliative and end-of-life care in hematologic malignancies: progress and opportunities. JCO Oncol Pract. 2024;20(6):739-741. https://doi.org/10.1200/OP.24.00081ArticlePubMed
- 32. Lee J, Jeong DS, Jeon H, Kim JH, Kim DY. Factors affecting intensive care unit nurses’ care burden of patients with hematologic neoplasm. Asian Oncol Nurs. 2022;22(4):235-244. https://doi.org/10.5388/aon.2022.22.4.235Article
- 33. Wu M, Gao H. A prediction model for in-hospital mortality in intensive care unit patients with metastatic cancer. Front Surg. 2023;10:992936. https://doi.org/10.3389/fsurg.2023.992936ArticlePubMedPMC
- 34. Seong JS, So HY. Comparative analysis of the accuracy of severity scoring systems for the prediction of healthcare outcomes of intensive care unit patients. J Korean Crit Care Nurs. 2015;8(1):71-79.
- 35. Zhang N, Lin Q, Jiang H, Zhu H. Age-adjusted Charlson comorbidity index as effective predictor for in-hospital mortality of patients with cardiac arrest: a retrospective study. BMC Emerg Med. 2023;23(1):7. https://doi.org/10.1186/s12873-022-00769-4ArticlePubMedPMC
- 36. Katircioglu K, Ayvat P, Gunturkun F. Cardiac arrest patients admitted to intensive care unit after cardiopulmonary resuscitation: a retrospective cohort study to find predictors for mortality. Braz J Anesthesiol. 2023;73(4):401-408. https://doi.org/10.1016/j.bjane.2021.03.013ArticlePubMedPMC
- 37. Haar M, Müller J, Hartwig D, von Bargen J, Daniels R, Theile P, et al. Intensive care unit cardiac arrest among very elderly critically ill patients: is cardiopulmonary resuscitation justified? Scand J Trauma Resusc Emerg Med. 2024;32(1):84. https://doi.org/10.1186/s13049-024-01259-1ArticlePubMedPMC
- 38. Kim JY, Kim JM, Kim Y. The effect of nutritional supply on clinical outcomes and nutritional status in critically ill patients receiving continuous renal replacement therapy. J Nutr Health. 2015;48(3):211-220. https://doi.org/10.4163/jnh.2015.48.3.211Article
- 39. Wei D, Sun Y, Chen R, Meng Y, Wu W. Age adjusted Charlson comorbidity index and in hospital mortality in critically ill patients with cardiogenic shock: a retrospective cohort study. Exp Ther Med. 2023;25(6):299. https://doi.org/10.3892/etm.2023.11998ArticlePubMedPMC
- 40. Ho MH, Liu HC, Joo JY, Lee JJ, Liu MF. Critical care nurses’ knowledge and attitudes and their perspectives toward promoting advance directives and end-of-life care. BMC Nurs. 2022;21(1):278. https://doi.org/10.1186/s12912-022-01066-yArticlePubMedPMC
- 41. Choi SJ, Kwon MS, Kim SH, Kim HM, Jung YS, Jo GY. Effects of using standardized patients on nursing competence, communication skills, and learning satisfaction in health assessment. J Korean Acad Soc Nurs Educ. 2013;19(1):97-105. https://doi.org/10.5977/jkasne.2013.19.1.97Article
- 42. Jang JE, Ryu JM, Heo MH, Kwon DE, Seo JY, Kim DY. Participation and influencing factors in the decision-making of life-sustaining treatment: a focus on deceased patients with hematologic neoplasms. J Hosp Palliat Care. 2023;26(2):69-79. https://doi.org/10.14475/jhpc.2023.26.2.69ArticlePubMedPMC
References
Figure & Data
REFERENCES
Citations

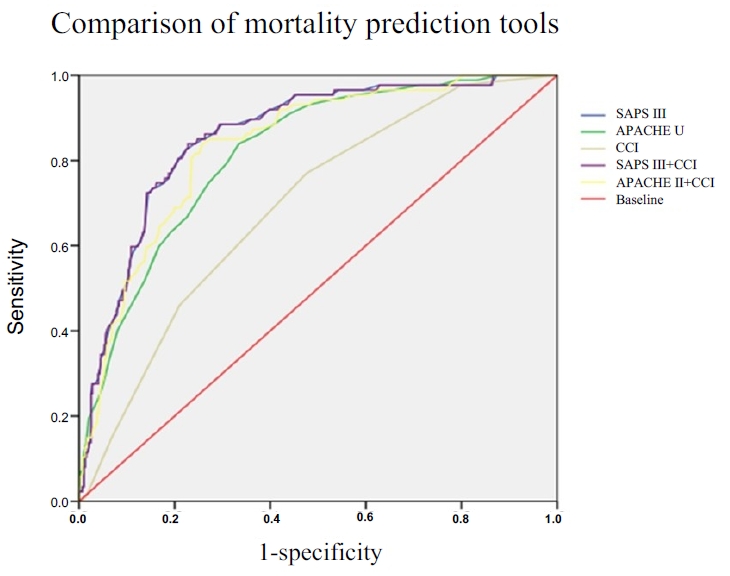
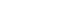
Fig. 1.
| Characteristic | Total (n=482) | Death (n=87) | Survival (n=395) | χ2 or t | p |
|---|---|---|---|---|---|
| Gender | 0.55 | .459 | |||
| Men | 299 (62.0) | 57 (65.5) | 242 (61.3) | ||
| Women | 183 (38.0) | 30 (34.5) | 153 (38.7) | ||
| Age (yr) | 2.71 | .745 | |||
| <40 | 37 (7.8) | 7 (8.0) | 30 (7.5) | ||
| 40–59 | 113 (23.4) | 23 (26.4) | 90 (22.8) | ||
| 60–69 | 124 (25.7) | 25 (28.7) | 99 (25.1) | ||
| 70–74 | 51 (10.6) | 10 (11.5) | 41 (10.4) | ||
| 75–79 | 59 (12.2) | 9 (10.3) | 50 (12.7) | ||
| ≥80 | 98 (20.3) | 13 (15.1) | 85 (21.5) | ||
| Mean age (yr) | 65.7±15.98 | 63.9±15.80 | 66.1±16.01 | 1.20 | .230 |
| BMI (kg/m2) | 0.62 | .892 | |||
| Underweight (<18.5) | 65 (13.5) | 12 (13.8) | 53 (13.4) | ||
| Normal (18.5–22.9) | 209 (43.4) | 40 (46.0) | 169 (42.8) | ||
| Overweight (23–24.9) | 99 (20.5) | 18 (20.7) | 81 (20.5) | ||
| Obese (≥25) | 109 (22.6) | 17 (19.5) | 92 (23.3) | ||
| Mean BMI | 22.59±4.02 | 22.29±3.39 | 22.65±4.15 | 0.77 | .443 |
| COVID-19 infection | 1.77 | .184 | |||
| Yes | 25 (5.2) | 7 (8.0) | 18 (4.6) | ||
| No | 457 (94.8) | 80 (92.0) | 377 (95.4) | ||
| Acute renal failure | 1.05 | .306 | |||
| Yes | 92 (19.1) | 20 (23.0) | 72 (18.2) | ||
| No | 390 (80.9) | 67 (77.0) | 323 (81.8) | ||
| Department | 56.30 | <.001 | |||
| Infection diseases | 27 (5.6) | 7 (8.0) | 20 (5.1) | ||
| Cardiology | 89 (18.5) | 10 (11.5) | 79 (20.0) | ||
| Nephrology | 26 (5.4) | 6 (6.9) | 20 (5.1) | ||
| General surgery | 52 (10.8) | 2 (2.3) | 50 (12.7) | ||
| Chest surgery | 45 (9.3) | 4 (4.6) | 41 (10.4) | ||
| Neurology | 19 (4.0) | 2 (2.3) | 17 (4.2) | ||
| Neuro-surgery | 60 (12.4) | 7 (8.0) | 53 (13.4) | ||
| Hemato-oncology | 68 (14.1) | 31 (35.6) | 37 (9.3) | ||
| Pulmonology | 58 (12.0) | 15 (17.2) | 43 (10.9) | ||
| Others | 38 (7.9) | 3 (3.5) | 35 (8.9) | ||
| Ventilator care | 61.74 | <.001 | |||
| Yes | 211 (43.8) | 71 (81.6) | 140 (35.4) | ||
| No | 271 (56.2) | 16 (18.4) | 255 (64.6) | ||
| ECMO | 15.91 | <.001 | |||
| Yes | 22 (4.6) | 11 (12.6) | 11 (2.8) | ||
| No | 460 (95.4) | 76 (87.4) | 384 (97.2) | ||
| CRRT | 52.28 | <.001 | |||
| Yes | 112 (23.2) | 46 (52.9) | 66 (16.7) | ||
| No | 370 (76.8) | 41 (47.1) | 329 (83.3) | ||
| CPCR | 117.54 | <.001 | |||
| Yes | 65 (13.5) | 43 (49.4) | 22 (5.6) | ||
| No | 417 (86.5) | 44 (50.6) | 373 (94.4) | ||
| LST | 174.32 | <.001 | |||
| Yes | 23 (4.8) | 21 (24.2) | 2 (0.5) | ||
| No | 420 (87.1) | 39 (44.8) | 381 (96.5) | ||
| DNR | 39 (8.1) | 27 (31.0) | 12 (3.0) | ||
| Inotropics | 178.12 | <.001 | |||
| Yes | 180 (37.3) | 87 (100.0) | 93 (23.5) | ||
| No | 302 (62.7) | 0 (0.0) | 302 (76.5) | ||
| Admission–ICU period | 8.08±13.12 | 14.85±18.41 | 6.59±11.13 | –4.02 | <.001 |
| ICU period | 9.29±10.81 | 12.19±10.95 | 8.65±10.68 | –2.79 | .005 |
| Admission route | 4.56 | .102 | |||
| Ward | 223 (46.2) | 41 (47.1) | 181 (45.9) | ||
| ICU | 59 (12.3) | 16 (18.4) | 43 (10.9) | ||
| ER | 200 (41.5) | 30 (34.5) | 171 (43.2) | ||
| Operation | 5.94 | .015 | |||
| Yes | 206 (42.7) | 27 (31.0) | 179 (45.3) | ||
| No | 276 (57.3) | 60 (69.0) | 216 (54.7) |
| Characteristic | Total (n=482) | Death (n=87) | Survival (n=395) | χ2 or t | p |
|---|---|---|---|---|---|
| SAPS III | 67.06±15.94 | 83.62±12.35 | 63.41±14.25 | –12.25 | <.001 |
| APACHE II | 17.51±7.97 | 24.99±7.06 | 15.87±7.18 | –10.76 | <.001 |
| CCI | 1.72 ± 1.23 | 2.37 ± 1.07 | 1.58 ± 1.22 | –5.57 | <.001 |
| Congestive heart failure | 1.57 | .211 | |||
| Yes | 124 (25.7) | 27 (31.0) | 97 (24.6) | ||
| No | 358 (74.3) | 60 (69.0) | 298 (75.4) | ||
| Dementia | 0.12 | .728 | |||
| Yes | 19 (3.9) | 4 (4.6) | 15 (3.8) | ||
| No | 463 (96.1) | 83 (95.4) | 380 (96.2) | ||
| Chronic pulmonary disease | 0.86 | .354 | |||
| Yes | 68 (14.1) | 15 (17.2) | 53 (13.4) | ||
| No | 414 (85.9) | 72 (82.8) | 342 (86.6) | ||
| Rheumatologic disease | 0.01 | .909 | |||
| Yes | 5 (1.0) | 1 (1.1) | 4 (1.0) | ||
| No | 477 (99.0) | 86 (98.9) | 391 (99.0) | ||
| Mild liver disease | 1.47 | .226 | |||
| Yes | 59 (12.2) | 14 (16.1) | 45 (11.4) | ||
| No | 423 (87.8) | 73 (83.9) | 350 (88.6) | ||
| Diabetes with chronic complication | 1.40 | .237 | |||
| Yes | 106 (22.0) | 15 (17.2) | 91 (23.0) | ||
| No | 376 (78.0) | 72 (82.8) | 304 (77.0) | ||
| Hemiplegia or paraplegia | 0.04 | .847 | |||
| Yes | 47 (9.8) | 8 (9.2) | 39 (9.9) | ||
| No | 435 (90.2) | 79 (90.8) | 356 (90.1) | ||
| Renal disease | 15.32 | <.001 | |||
| Yes | 198 (41.1) | 52 (59.8) | 146 (37.0) | ||
| No | 284 (58.9) | 35 (40.2) | 249 (63.0) | ||
| Leukemia and lymphoma | 43.73 | <.001 | |||
| Yes | 105 (21.8) | 42 (48.3) | 63 (15.9) | ||
| No | 377 (78.2) | 45 (51.7) | 332 (84.1) | ||
| Moderate or severe liver disease | 2.19 | .139 | |||
| Yes | 65 (13.5) | 16 (18.4) | 49 (12.4) | ||
| No | 417 (86.5) | 71 (81.6) | 346 (87.6) | ||
| Metastatic solid tumor | 6.18 | .013 | |||
| Yes | 32 (6.6) | 11 (12.6) | 21 (5.3) | ||
| No | 450 (93.4) | 76 (87.4) | 374 (94.7) | ||
| AIDS | .180a) | ||||
| Yes | 1 (0.2) | 1 (1.1) | 0 (0.0) | ||
| No | 481 (99.8) | 86 (98.9) | 395 (100.0) |
| Mortality prediction models | C-statistics | pa) |
|---|---|---|
| SAPS III | .857 | .576 |
| APACHE II | .817 | .729 |
| CCI | .692 | .118 |
| SAPS III+CCI | .857 | .543 |
| APACHE II+CCI | .834 | .128 |
| Variables (reference) | B | SE | p | OR (95% CI) | Tolerance | VIF |
|---|---|---|---|---|---|---|
| (constant) | –8.50 | 1.05 | <.001 | 0.01 | ||
| Ventilator care (no) | 0.64 | 0.39 | .100 | 1.90 (0.88–4.09) | .70 | 1.44 |
| CPCR (no) | 2.37 | 0.41 | <.001 | 10.67 (4.81–23.67) | .78 | 1.28 |
| CRRT (no) | 0.97 | 0.37 | .008 | 2.64 (1.29–5.40) | .79 | 1.27 |
| ECMO (no) | 0.56 | 0.64 | .381 | 1.75 (0.50–6.09) | .90 | 1.11 |
| Leukemia and lymphoma (no) | 1.41 | 0.38 | <.001 | 4.11 (1.95–8.65) | .79 | 1.27 |
| SAPS III | 0.06 | 0.02 | <.001 | 1.07 (1.03–1.10) | .35 | 2.85 |
| APACHE II | 0.04 | 0.03 | .189 | 1.04 (0.98–1.11) | .43 | 2.34 |
| CCI | –0.17 | 0.16 | .290 | 0.84 (0.61–1.16) | .68 | 1.48 |
Values are presented as number (%) or mean±standard deviation. BMI, body mass index; COVID-19, coronavirus disease 2019; CPCR, cardiopulmonary cerebral resuscitation; CRRT, continuous renal replacement therapy; DNR, do not resuscitate; ECMO, extracorporeal membrane oxygenation; ER, emergency room; ICU, intensive care unit; LST, life-sustaining treatment.
Values are presented as mean±standard deviation or number (%). AIDS, Acquired immune deficiency syndrome; APACHE, Acute Physiology and Chronic Health Evaluation; CCI, Charlson comorbidity index; SAPS, Simplified Acute Physiology Score. a)By Fisher’s exact probability test.
APACHE, Acute Physiology and Chronic Health Evaluation; CCI, Charlson comorbidity index; CPCR, cardiopulmonary cerebral resuscitation; CRRT, continuous renal replacement therapy; ECMO, extracorporeal membrane oxygenation; SAPS, Simplified Acute Physiology Score. a)By Hosmer-Lemeshow.
Nagelkerke R2=0.57, χ2=208.08, APACHE, Acute Physiology and Chronic Health Evaluation; CCI, Charlson Comorbidity Index; CI, confidence interval; CPCR, cardiopulmonary cerebral resuscitation; CRRT, continuous renal replacement therapy; ECMO, extracorporeal membrane oxygenation; OR, odds ratio; SAPS, Simplified Acute Physiology Score; SE, standard error; VIF, variance inflation factor.
 KSNS
KSNS
 Submit an article
Submit an article
 ePub Link
ePub Link Cite
Cite